[EXPLICANDO A MATÉRIA] Diagrama de Fases

No Explicando A Matéria de hoje, traremos alguns conceitos básicos sobre o Diagrama de Fases. A importância da sua compreensão se dá pelo conhecimento dos procedimentos utilizados em tratamentos térmicos, pois algumas das propriedades dos materiais estão relacionadas com o desenvolvimento das suas microestruturas. Além disso, os diagramas fornecem informações importantes a respeito dos fenômenos da fusão, fundição e cristalização, entre outros.
Para a interpretação do diagrama de fases, é necessário ter em mente alguns conceitos relacionados às ligas, fases e equilíbrio. O termo componente, por exemplo, é constantemente abordado nesse estudo, trata-se de metais puros e/ou compostos que compõem uma liga, assim, os componentes do latão são o cobre e o zinco. Outro termo usado com frequência é sistema, que no caso possui dois significados, podendo se referir a um corpo específico do material (como um cadinho de aço fundido), ou estar relacionado a uma série de possíveis ligas compostas pelos mesmos componentes, porém, independente da composição da liga (como o sistema ferro-carbono). E como visto anteriormente em um post do Explicando A Matéria, a solução sólida, usualmente designada nos diagramas por letras gregas minúsculas.
Já o limite de solubilidade, trata-se de uma concentração máxima de átomos de soluto que podem ser dissolvidos no solvente em uma dada temperatura. Muitos sistemas de ligas possuem esse limite, dessa forma, é representado no diagrama de temperatura pela composição, onde a composição corresponde a intersecção de uma temperatura específica com a linha do limite de solubilidade (linha solvus).
Uma fase pode ser definida como uma parcela homogênea de um sistema que possui características físicas e químicas uniformes. Dado um sistema, se mais de uma fase estiver presente, cada uma terá suas propriedades, sendo separadas por uma fronteira. O equilíbrio de fases está relacionado a um valor mínimo de energia livre, dependente de uma combinação de temperatura, pressão e composição específicas. O termo equilíbrio de fases se refere aos sistemas heterogêneos - duas ou mais fases, sendo uma constância nas características das fases ao longo do tempo.
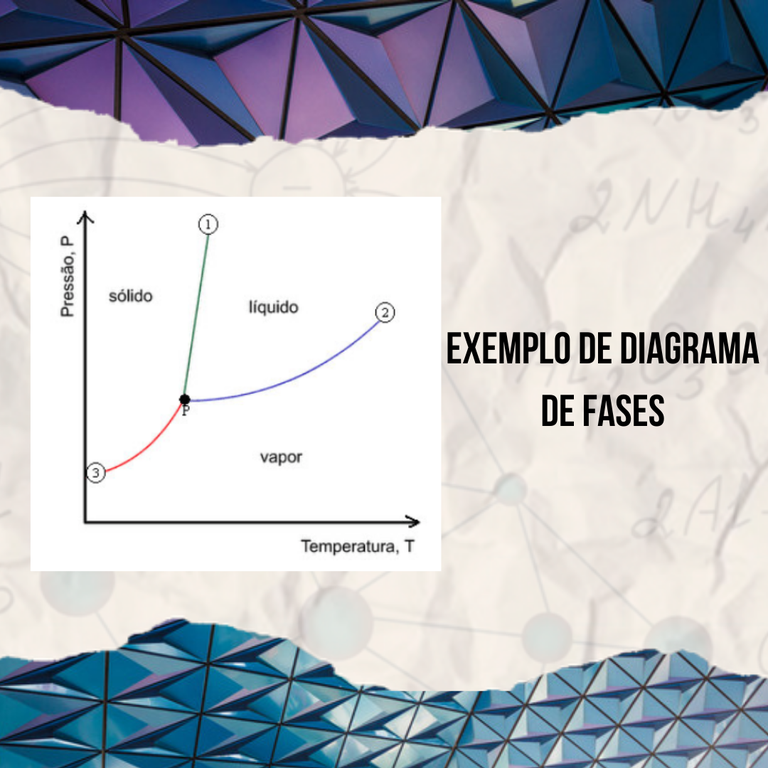
Através do diagrama de fases, é possível obter informações a respeito do controle da estrutura das fases de um determinado sistema. Existem três parâmetros externos que impactam no desenvolvimento da estrutura das fases - temperatura, pressão e composição, assim, os diagramas são construídos por meio da combinação desses parâmetros. O diagrama de fases mais simples é aquele para um sistema de um único componente, assim, somente a pressão e a temperatura são variáveis, dessa maneira, é representado pela pressão no eixo das ordenadas e pela temperatura no eixo das abscissas. Por exemplo, para o diagrama H2O, é possível observar três fases - sólido, líquido e gasoso, onde cada uma existe por determinada condição de equilíbrio temperatura-pressão, separadas por três curvas. Também é possível observar que todas as três curvas das fronteiras se interceptam no ponto O, denominado ponto invariante, este representa um equilíbrio simultâneo de todas as fases, no qual qualquer alteração de temperatura e/ou pressão acarreta no desaparecimento de uma das fases.
Outro tipo de diagrama existente, é aquele no qual a temperatura e a composição são os parâmetros variáveis, sendo a pressão mantida constante (normalmente 1 atm), como os diagramas de fases de ligas binárias. Esses são mapas que representam a relação existente entre temperatura e composição das fases em equilíbrio, sendo úteis para prever as microestruturas, pois muitas se desenvolvem a partir das transformações de fase. O diagrama de fases binário mais fácil de ser analisado é o sistema cobre-níquel, que possui três fases: alfa - solução sólida substitucional, líquido (L) - solução líquida homogênea, e bifásico (alfa+L), separados pela linha liquidus e solidus, respectivamente. É considerado um sistema isomorfo devido a completa solubilidade dos componentes, tanto no estado sólido, como no líquido.
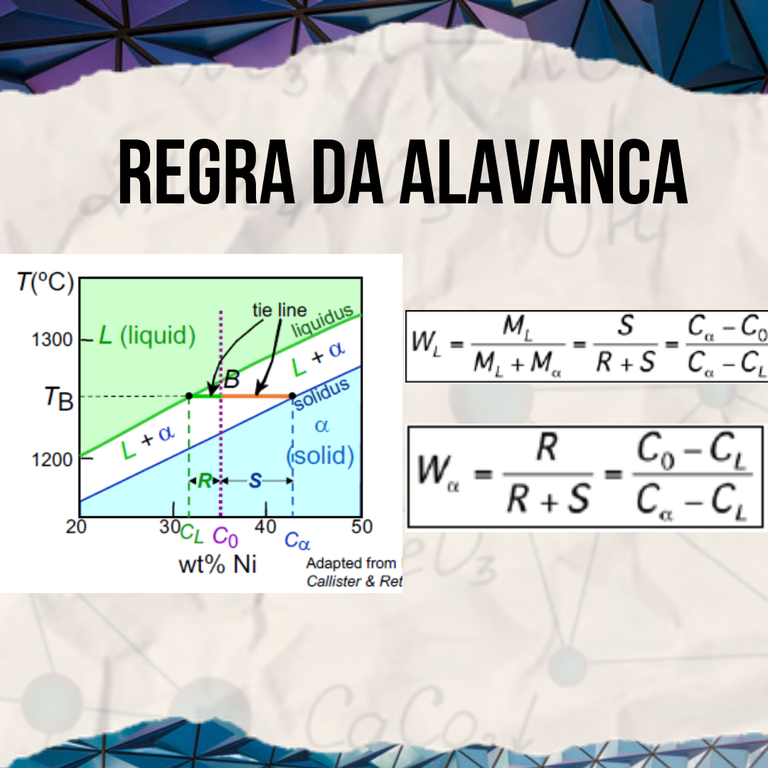
Em sistemas binários que estejam em equilíbrio, é possível obter pelo menos três informações, sendo elas as fases presentes, as composições de cada fase (porcentagem em peso) e suas respectivas frações. Para regiões bifásicas, é possível determinar as quantidades das fases através de um conjunto de procedimentos, denominado regra da alavanca, baseada na razão entre os comprimentos dos segmentos da linha de amarração.
Outra informação relevante, é que para alguns sistemas de ligas podem ser encontradas soluções sólidas intermediárias, existentes em composições que não estão localizadas nos extremos das composições. Já para sistemas metal-metal, são encontrados compostos intermediários discretos, denominados intermetálicos, cuja fórmula química é específica.
As transformações de fases são classificadas de acordo com a mudança ou não na composição das fases envolvidas. Assim, aquelas que não possuem alterações na composição são denominadas transformações congruentes, por exemplo, a fusão de materiais puros. Caso uma das fases apresente uma mudança na composição, é denominada incongruente, como as reações eutéticas, eutetóides, peritéticas e peritetóides, além da fusão de uma liga que possui sistema isomorfo.

Fonte: CALLISTER, W. D.,Ciência e Engenharia de Materiais: Uma Introdução. John Wiley & Sons, Inc., 2002.
t.png)